Материалы, которые не подвержены обледенению, были бы очень востребованы в авиастроении, техническом обслуживании автомобильных дорог и линий электропередач, строительстве и во многих других областях человеческой деятельности. К сожалению, такие вещества пока не созданы. Существующие методы борьбы с обледенением либо очень энергоемки, либо наносят вред окружающей среде. Американские ученые из Висконсинского и Гарвардского университетов, исследовав динамику столкновения капель воды с различными холодными поверхностями (температура меньше 0°C), предложили идею, как можно преодолеть это природное явление. Проведенные эксперименты показывают, что, используя сверхгидрофобные вещества (сильно отталкивающие воду) с искусственно созданными на их поверхности наноструктурами, можно предотвратить изначальный рост льда на них и избежать обледенения.
Большинство инфраструктурных объектов, используемых человечеством, остаются уязвимыми для такого природного явления, как обледенение. Распространяясь по какой-либо поверхности в виде даже очень тонкого слоя, лед способен разрывать линии электропередач, разрушать трубопроводы, делать дороги непроходимыми, значительно уменьшать подъемную силу самолета и т. д. Образовавшаяся ледяная корка настолько прочна, что ликвидировать ее на больших территориях очень сложно, а то и невозможно.
Самый распространенный способ избавления от льда — плавление. Однако существующие для этого физические и химические методы сопряжены с определенными проблемами. Прежде всего, из-за значительной удельной энергии плавления льда на нагревание надо затратить большое количество энергии. К тому же, в случае разной толщины льда, трудно оценить продолжительность нагревания. Определение «на глаз» создает серьезный риск разрушения поверхности и опять-таки требует значительных энергетических затрат. Соль, уменьшающая температуру кристаллизации воды, приводит к коррозии поверхностей и наносит вред экологии. Этиленгликоль (еще одно вещество, используемое в борьбе с обледенением) токсичен.
Однако ученые не оставляют попыток разработать эффективную методику противостояния ледяной угрозе. Для этого они детально изучают процесс формирования льда на поверхности различных веществ. Им удалось обнаружить, что образование пресловутой ледяной корки начинается с взаимодействия капель воды с поверхностью, на которой они находятся. Следовательно, предупреждать обледенение можно, если каким-то образом научиться создавать поверхности, которые не только не позволяли бы каплям замерзать, но и вообще отталкивали бы их от себя.
Механизм отталкивания воды и водяных капель уже давно используется в природе. Его применяют более 200 видов растений (хорошо известен эффект лотоса) и различные животные (например, водомерки). Все эти живые организмы имеют в своем распоряжении поверхности, сильно и очень сильно отталкивающие от себя воду. Такое «неприятие» воды называется соответственно гидрофобностью и сверхгидрофобностью. Возникает оно не только благодаря определенным физико-химическим характеристикам материалов, но и, как выяснилось, за счет «хитрой» геометрической структуры их поверхности.
Хорошей иллюстрацией природного использования структурированных микрошероховатостей с целью улучшения водоотталкивающих свойств может служить лист растения таро (Colocasia esculenta). На снимке (рис. 1), сделанном с помощью сканирующего электронного микроскопа, хорошо видны упорядоченные структуры на поверхности сверхгидрофобного листа этого растения.
Чтобы выяснить, как геометрия поверхности может помочь в решении проблемы обледенения, ученые из Висконсинского и Гарвардского университетов США исследовали динамику столкновения капель воды со сверхгидрофобным материалом при положительной и отрицательной температуре. Исходя из полученных результатов, они выдвинули гипотезу, согласно которой «правильно» сконструированные наноструктуры на поверхности сверхгидрофобного вещества способны отталкивать воду вплоть до –30°C, предотвращая тем самым образования ледяной корки.
Гидрофильность, гидрофобность и сверхгидрофобность
Представим себе, что на абсолютно гладкой поверхности материала (подложке) находится капля воды. Между водой и поверхностью будет возникать межмолекулярное взаимодействие, которое называется смачиванием.
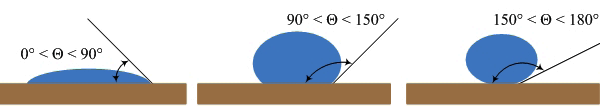
Количественно это явление характеризуется краевым углом (углом смачивания). Это угол между поверхностью и касательной плоскостью, проведенной к границе раздела системы «капля жидкости — поверхность — окружающая среда». По величине краевого угла судят о характере взаимодействия капли с поверхностью (рис. 2). Если краевой угол находится в пределах от 0° до 90°, то поверхность называется гидрофильной (сильное смачивание). Форма капли на гидрофильной поверхности определяется краевым углом: чем меньше краевой угол, тем сильнее растекается капля и тем больше площадь ее контакта с подложкой. При краевом угле от 90° до 150° поверхность считается гидрофобной (слабое смачивание). В этом случае капля воды стремится принять форму, близкую к шарообразной, поэтому площадь ее контакта с гидрофобной поверхностью невелика. Когда же угол смачивания превышает 150° (и, естественно, не превосходит 180°), капля едва соприкасается с поверхностью (представляет собой почти шар). Такие поверхности называются сверхгидрофобными (смачивание практически отсутствует).
Описанные типы взаимодействия капли с поверхностью, как и многие другие физические явления, обусловлены принципом минимума энергии: капля стремится принять форму с минимально возможным значением энергии. Один из «источников» энергии капли (если она не очень большая, иначе нужно учитывать еще и силу тяжести) — взаимодействие молекул воды между собой и взаимодействие поверхности с близлежащими молекулами воды. Если сила межмолекулярного взаимодействия между молекулами воды внутри капли слабее взаимодействия между молекулами воды и поверхности, то капле энергетически выгодно растечься (то есть сформировать острый краевой угол). Так возникает явление гидрофильности.
Когда молекулы воды внутри капли сцеплены сильнее, чем сила, с которой они контактируют с поверхностью, капле выгоднее иметь форму, близкую к шару В этом случае реализуется гидрофобность. Сверхгидрофобность означает, что молекулы воды практически не обращают внимания на силы, действующие со стороны подложки. Для обеспечения минимума энергии капли молекулам воды лучше всего взаимодействовать только между собой.
Всё вышесказанное относится к идеально гладкой поверхности. В действительности же любая поверхность, даже кажущаяся гладкой, имеет наноскопические и микроскопические шероховатости. Многочисленные эксперименты установили, что этот нано- и микрорельеф способен существенно менять краевой угол и делать его неоднозначным в определении (специалисты называют это гистерезисом смачивания). Поэтому свойства поверхности в отношении попадающей на нее воды могут существенно меняться: например, гидрофобная поверхность может стать сверхгидрофобной. Происходит это, во-первых, потому, что шероховатости увеличивают площадь взаимодействия поверхности с каплей. А во-вторых, форма микрорельефа влияет на то, как капля после попадания на поверхность будет растекаться по ней.
Учет второй причины в теоретических моделях, описывающих растекание капли, до сих пор представляет собой сложную задачу. Очевидно, что распределение шероховатостей по поверхности носит, как правило, случайный характер. Однако для простоты дальнейшего изложения будет считать, что они образуют регулярную сетку из нано- или микроскопических столбов.
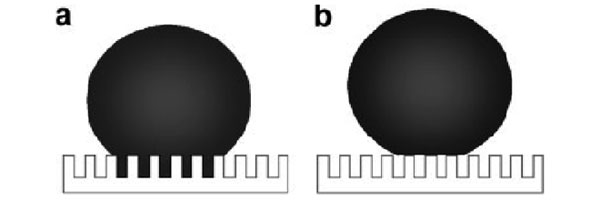
На рис. 3 показаны два основных типа расположения капли на сверхгидрофобной шероховатой поверхности: состояние Венцеля (рис. 3а) и состояние Кассье (рис. 3b). В состоянии Венцеля капля частично смачивает шероховатые области, и поэтому заполняет их водой. В состоянии Кассье капля не реагирует на рельеф поверхности и не смачивает участки с шероховатостями, имея меньшую площадь контакта.
Что нового?
То, что изначально гидрофобная поверхность при нанесении на нее специальных наноструктур усиливает свои водоотталкивающие свойства, становясь сверхгидрофобной, для ученых секретом не было. Эта уловка уже активно используется при создании сверхгидрофобных поверхностей.
Новизна этой работы в том, что подавляющее большинство опубликованных статей о влиянии рельефа на сверхгидрофобность относятся лишь к взаимодействию неподвижных (статичных) капель с поверхностью. О том, как происходит этот процесс в динамике, известно очень мало. Кроме того публикации с подобными экспериментами содержат изыскания, проведенные при комнатной температуре. Однако задавшись целью выяснить, как сверхгидрофобная поверхность и наноструктуры на ней могут помочь в борьбе с обледенением, необходимо проследить и изучить во времени процесс столкновения капель воды с подложкой, температура которой меньше 0°C. Именно это и было впервые проделано авторами обсуждаемой здесь статьи.
Для этого ученые изготовили сверхгидрофобную поверхность из фторированного кремния, на которую литографическим образом нанесли разного рода и разного размера упорядоченные наноструктуры (рис. 4). Далее они провели серию экспериментов, в которых наблюдали падение капель объемом 15 мкл (радиус несколько миллиметров) с высоты 10 см на кремниевую подложку, температура которой варьировалась от +20°C до –35°C. Температура капель также не была константой и менялась в пределах от –5°C (переохлажденная капля) до +60°C.
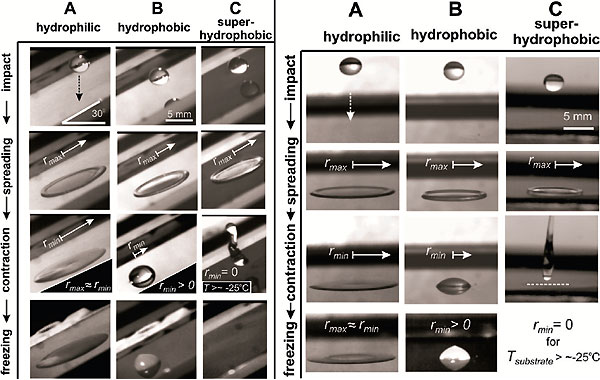
В ходе экспериментов ученые получили еще один очень важный результат. Приземлившись на сверхгидрофобную поверхность, капля находится в состоянии Кассье. Почему этот факт так важен? Предположим, что капля всё-таки ухитрилась замерзнуть на сверхгидрофобной поверхности. Теперь еще раз взглянем на рис. 3b, который иллюстрирует состояние Кассье. Видно, что вода не проникает непосредственно вглубь шероховатостей и потому, в отличие от состояния Венцеля, имеет маленькую площадь соприкосновения со сверхгидрофобной подложкой. Следовательно, с такой поверхности можно относительно легко убрать замороженную каплю (см. видео), не оставив никаких ледяных следов.
Наконец, ученые выяснили, что наноструктурированные сверхгидрофобные поверхности проявляют высокую гидростатическую и гидродинамическую устойчивость. Максимальное давление, при котором поверхность сохраняет свои сверхгидрофобные свойства (то есть краевой угол капли остается неизменным) достигает 40–60 атмосфер. Это эквивалентно давлению, которое оказывали бы капли, падающие на эту поверхность со скоростью 90–135 м/с. Правда, приведенные данные относятся лишь к структурам на поверхности, имеющим так называемую «закрытую» геометрию — например, в виде кирпичиков или пчелиных сот. Для «открытых» геометрий типа сетки столбиков значения будут меньше. Главная причина такой зависимости связана с тем, что капли, находящиеся на геометрически закрытых наноструктурах, способны герметично удержать под собой воздух, который амортизирует внешнее давление. Наконец, немаловажен и тот факт, что поверхности с закрытой геометрией технологически легче изготавливать.
Так что надо противостоять не обледенению, а предшествующим ему событиям. Авторы надеются, что проделанная ими работа поможет по-новому взглянуть на тактику борьбы с образованием льда на различных поверхностях.
Мои любимые тесты - Определите свой уровень тревоги и депрессии! Мне кажется, что я больна! Если мне не отвечает мой любимый человек сутки и более, то я в конвульсиях рыдаю.


